의료기기 제조 및 수입품목허가(인증, 신고, 인허가)
1. 처리기간
가. 임상시험 검토대상 : 80일
나. 기술문서 검토대상 : 65일
다. 기술문서 등 심사불필요 : 10일
2. 구비서류
가. 동등·개량·새로운 제품일 경우
1) 의료기기 수입(제조)허가 신청서
2) 허가신청 구비서류
3) 기술문서 심사 결과통지서 (발행일로부터 2년이 경과되지 아니한 것)
나. 동등공고제품일 경우
1) 의료기기 수입(제조)허가 신청서
2) 허가신청 구비서류
3) 식약처장이 지정한 시험검사기관에서 발급한 동등공고제품 시험성적서
다. 동일제품일 경우 (수입품목 허가의 경우)
1) 의료기기 수입(제조)품목허가 신청서
2) 허가신청 구비서류
3) 의료기기정책과에서 발급한 동일제품임을 증명하는 공문
3. 허가신청서 기재항목
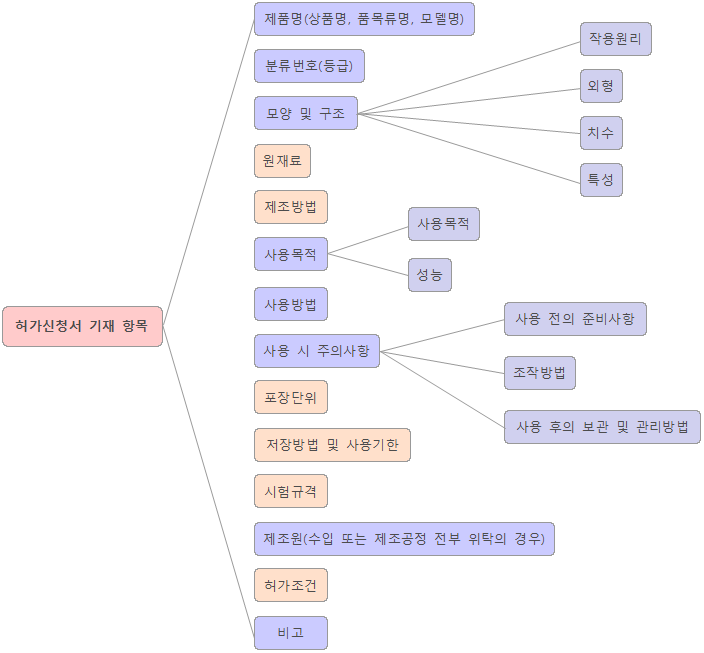
4. 기술문서 심사를 위한 제출 자료
가. 이미 허가받은 제품과 비교한 자료
나. 사용목적에 관한 자료
다. 작용원리에 관한 자료
라. 제품의 성능 및 안전을 확인하기 위한 자료
1) 전기·기계적 안전에 관한 자료
2) 생물학적 안전에 관한 자료
3) 방사선에 관한 안전성 자료
4) 전자파장해에 관한 자료
5) 성능에 관한 자료
6) 물리․화학적 특성에 관한 자료
7) 안정성에 관한 자료
마. 기원 또는 발견 및 개발경위에 관한 자료
바. 임상시험에 관한 자료
사. 외국의 사용현황 등에 관한 자료
